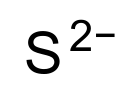Sulfide (hệ thống tên
sulfanediide , và
sulfide (2-) ) (
British English sunfua ) là một
chất vô cơ anion của
lưu huỳnh với công thức hóa học S
2- . Nó góp phần không màu thành sunfit muối. Vì nó được phân loại là một
nền tảng vững chắc , thậm chí pha loãng dung dịch của muối như
natri sunfua (Na
2 S) là ăn mòn và có thể tấn công da. Sulfide là anion lưu huỳnh đơn giản nhất.
Danh pháp [ sửa ]
Tên hệ thống
sulfanediide và
sulfide (2-) , hợp lệ
IUPAC tên, được xác định theo các danh mục của substitutive và phụ gia, tương ứng. Tuy nhiên, tên sulfide cũng được sử dụng trong thành phần IUPAC danh pháp mà không mất bản chất của liên kết liên quan. Ví dụ về cách đặt tên như vậy là
selen disulfua và
sulfide titan , mà không chứa ion sulfide nào.
Sulfide cũng được sử dụng không có hệ thống, để mô tả các hợp chất mà phóng
hydrogen sulfide khi axit hóa, hoặc một hợp chất mà nếu không kết hợp lưu huỳnh trong một số hình thức, chẳng hạn như
dimethyl sulfide . "Hydrogen sulfide" chính nó là một ví dụ về một tên không có hệ thống của thiên nhiên này. Tuy nhiên, nó cũng là một cái tên tầm thường, và tên IUPAC ưa thích dành cho
sulfane .
Tính chất hóa học [ sửa ]
Sulfide không tồn tại trong nồng độ đáng kể ngay cả trong nước có tính kiềm cao, là không thể phát hiện ở pH <~ 15 (8 M
NaOH ).
[2]
Tánh chất diêm cơ [ sửa ]
Các anion sulfide có thể đồng hóa một proton bằng tái tổ hợp:
- S 2- + H + → SH -
Vì chụp này của một proton (H
+ ), sulfua có tính cách cơ bản. Trong dung dịch nước, nó có một
p K b giá trị nhỏ hơn 0. của
axit liên hợp là
bisulfide (SH
- ). Trong dung dịch nước, hầu hết các ion sulfide được vô hiệu hóa.
- S 2- + H 2 O SH - + OH -

Phản ứng hóa học [ sửa ]
- 8 8 MGS + I 2 → S 8 + 8 MGI 2
Lưu huỳnh cũng có thể được điều chế từ một sulfide và chất ôxy hóa thích hợp:
- 16 HNO 3 + 24 H 2 S → 16 NO + 3 S 8 + 32 H 2 O
Các dẫn xuất kim loại [ sửa ]
Dung dịch nước của
quá trình chuyển đổi kim loại cation phản ứng với nguồn sulfua (H
2 S, NaHS, Na
2 S) để kết tủa sulfide rắn. Như vậy
vô cơ sulfide thường có khả năng hòa tan rất thấp trong nước, và nhiều người liên quan đến khoáng sản với các thành phần tương tự (xem dưới đây). Một ví dụ nổi tiếng là CdS loài vàng tươi hoặc "
cadmium vàng ". Các xỉn đen hình thành trên bạc sterling là Ag
2 loài S. như vậy đôi khi được gọi là muối. Trong thực tế, các liên kết trong các sulfua kim loại chuyển tiếp được đánh giá cao kết cộng hóa trị, mà làm phát sinh của họ
bán dẫn thuộc tính, do đó có liên quan đến màu sắc sâu. Một số có ứng dụng thực tế như bột màu, trong các tế bào năng lượng mặt trời, và như chất xúc tác.
Aspergillus niger đóng một vai trò trong việc hòa tan các sunfua kim loại nặng.
[3]
Địa chất [ sửa ]
Ăn mòn gây ra bởi sulfide [ sửa ]
Hòa tan sulfide miễn phí (H
2 S, HS
- và S
2- ) là loài rất hung hăng đối với sự ăn mòn của nhiều kim loại như thép, thép không gỉ, và đồng. Sulfide có mặt trong dung dịch nước chịu trách nhiệm về
sự ăn mòn căng thẳng nứt (SCC) của thép, và còn được gọi là
căng thẳng sulfide nứt . Ăn mòn là một mối quan tâm lớn trong nhiều sulfide xử lý cài đặt công nghiệp: nhà máy quặng sulfide, sâu
giếng dầu , đường ống vận chuyển trở nên xấu đi
dầu ,
giấy Kraft các nhà máy.
Ăn mòn vi khuẩn có gây ra (MIC) hoặc
sulfide ăn mòn hữu cơ cũng được gây ra bởi
vi khuẩn giảm sulfate sản xuất sulfide được phát ra trong không khí và oxy hóa trong axit sulfuric do vi khuẩn lưu huỳnh oxi hóa. Axit sulfuric hữu cơ phản ứng với
nước thải vật liệu và thường nhất gây mất đoàn thể, các vết nứt trên các đường ống thoát nước và cuối cùng là sự sụp đổ cơ cấu. Đây là loại suy thoái là một quá trình quan trọng ảnh hưởng đến hệ thống thoát nước trên toàn thế giới và dẫn đến chi phí phục hồi rất cao.
Quá trình oxy hóa của sulfide cũng có thể hình thành
thiosulfate (
S
2 O 2-
3 ) một loài trung gian chịu trách nhiệm về các vấn đề nghiêm trọng của
rỗ ăn mòn của thép và thép không gỉ trong khi các phương tiện truyền cũng được axit hóa bằng việc sản xuất axit sulfuric khi quá trình oxy hóa là nâng cao hơn.
Hóa hữu cơ [ sửa ]
Trong
hóa học hữu cơ , "sulfide" thường dùng để chỉ các mối liên kết C-S-C, mặc dù thuật ngữ
thiôête ít mơ hồ. Ví dụ, thiôête
dimethyl sulfide là CH
3 -S-CH
3 .
Polyphenylene sulfide (xem dưới đây) có kinh nghiệm công thức C
6 H
4 S. Thỉnh thoảng, những sulfide hạn đề cập đến các phân tử chứa -SH
nhóm chức năng . Ví dụ, methyl sulfide có thể có nghĩa là CH
3 -SH. Các mô tả ưa thích dành cho các hợp chất SH-chứa như vậy là
thiol hoặc mercaptan, tức là methanethiol hoặc methyl mercaptan.
Disunphua [ sửa ]
Lẫn lộn phát sinh từ các ý nghĩa khác nhau của thuật ngữ "
disulfua ".
Molybdenum disulfide (MoS
2 ) bao gồm các trung tâm sulfide tách ra, gắn với molypden trong chính thức 4 trạng thái ôxi hóa (Mo
4+ ). Sắt disulfua (
pyrit , FeS
2 ) Mặt khác bao gồm S
2 2- , hoặc
- S-S
- dianion, gắn với sắt hóa trị hai trong 2 trạng thái ôxi hóa (ion sắt: Fe
2+ ).
Dimethyldisulfide có hóa ràng buộc CH
3 -S-S-CH
3 , trong khi
cacbon disulfua không có trái phiếu S-S, là S = C = S (tuyến tính phân tử tương tự để CO
2 ). Thường xuyên nhất trong hóa học lưu huỳnh và hóa sinh, thuật ngữ disulfua thường được gán cho các tín hiệu tương tự lưu huỳnh của
peroxide trái phiếu -O-O-. Các
disulfua trái phiếu (-S-S) đóng một vai trò quan trọng trong cấu tạo của
protein và hoạt tính xúc tác của
enzyme .
Ví dụ [ sửa ]
|
| H 2 S | Hydrogen sulfide là một loại khí rất độc hại và ăn mòn đặc trưng bởi một mùi đặc trưng của "trứng thối". | −85.7 | −60.20 | 7783-06-4 |
| Băng đĩa | Cadmium sulfide có thể được sử dụng trong tế bào quang điện . | 1750 | | 1306-23-6 |
| Canxi polysulfide ( " vôi lưu huỳnh ") là một truyền thống loại thuốc diệt nấm trong vườn . | | | |
| CS 2 | Carbon disulfide đôi khi được sử dụng như một dung môi trong hóa học công nghiệp. | −111.6 | 46 | 75-15-0 |
| PBS | Sulfide Chì được sử dụng trong tia hồng ngoại cảm biến. | 1114 | | 1314-87-0 |
| MoS 2 | Molybdenum disulfide , các khoáng molybdenit , được sử dụng như một chất xúc tác để loại bỏ lưu huỳnh từ nhiên liệu hóa thạch; cũng như chất bôi trơn cho các ứng dụng nhiệt độ cao và áp suất cao. | | | 1317-33-5 |
| Cl-CH 2 CH 2 -S-CH 2 CH 2 -Cl | Lưu huỳnh mù tạt (mustard gas) là một organosulfide (thiôête) đã được sử dụng như một vũ khí hóa học trong chiến tranh thế giới thứ nhất, clorua trên phân tử đóng vai trò như một nhóm ra khi có sự hiện diện của nước và tạo thành một thiôête cồn và HCl . | 13–14 | 217 | 505-60-2 |
| Tại 2 S | Bạc sunfua được hình thành trên bạc danh bạ điện hoạt động trong một môi trường giàu hydrogen sulfide . | | | 21548-73-2 |
| Na 2 S | Natri sunfua là một hóa chất công nghiệp quan trọng, được sử dụng trong sản xuất giấy kraft giấy , thuốc nhuộm , thuộc da , dầu thô chế biến, xử lý kim loại nặng ô nhiễm , và những người khác. | 920 | 1180 | 1313-82-2 |
| ZnS | Kẽm sulfua được sử dụng cho ống kính và khác quang thiết bị trong hồng ngoại một phần của quang phổ . Kẽm sulfua pha tạp với bạc được sử dụng trong máy dò alpha trong khi kẽm sulfide với dấu vết của đồng có ứng dụng trong photoluminescent dải chiếu sáng khẩn cấp và quay đồng hồ dạ quang. | | 1185 | 1314-98-3 |
| MES | Một vài sulfua kim loại được sử dụng như các chất màu trong nghệ thuật, mặc dù sử dụng của họ đã giảm phần nào do độc tính của họ. Sắc tố sulfide bao gồm cadmium, thủy ngân, asen và. | | | |
| C 6 H 4 S | Sulfide Polyphenylene là một polymer thường được gọi là "Sulfar". Đơn vị lặp lại của nó được liên kết với nhau bởi sulfide (thiôête) liên kết. | | | 26125-40-6
25212-74-2 |
| SES 2 | Selenium disulfua là một kháng nấm được sử dụng trong chế phẩm chống gàu, chẳng hạn như Selsun xanh . Sự hiện diện của selen có độc tính cao trong chăm sóc sức khỏe và mỹ phẩm sản phẩm đại diện cho một sức khỏe nói chung và mối quan tâm về môi trường. | <100 | | 7488-56-4 |
| ch 2 | Các mạng tinh thể của pyrit được làm bằng disulfua sắt , trong đó sắt là hóa trị hai và trình bày như là ion sắt (Fe 2+ ). | 600 | | 1317-66-4 |
Chuẩn bị [ sửa ]
Hợp chất sulfide có thể được chuẩn bị theo những cách khác nhau:
[5]
- kết hợp trực tiếp của các yếu tố:
- Ví dụ: Fe (s) + S (s) → FeS (s)
- Giảm một sunfat:
- Ví dụ: MgSO 4 (s) + 4C (s) → MGS (s) + 4CO (g)
- Lượng mưa của một sulfide không hòa tan:
- Ví dụ: M 2+ + H 2 S (g) → MS (s) + 2H + (aq)
An toàn [ sửa ]
Nhiều sulfua kim loại rất không tan trong nước mà họ có thể không phải là rất độc hại. Một số sulfua kim loại, khi tiếp xúc với một khoáng chất mạnh
axit , bao gồm
axit dạ dày , sẽ phát hành độc
hydrogen sulfide .
Sulfide hữu cơ là rất dễ cháy. Khi một sulfide đốt cháy nó tạo ra
lưu huỳnh đioxit (SO
2 ) khí.
Hydrogen sulfide, một số muối của nó, và gần như tất cả các sulfua hữu cơ có mùi hôi thối mạnh mẽ và thối rữa; thối rữa
sinh khối phát hành này.
glycopeptide
Từ Wikipedia, bách khoa toàn thư miễn phí
Các
tổng hợp của glycopeptide cung cấp đầu dò sinh học cho các nhà nghiên cứu để làm sáng tỏ chức năng polisacarit trong tự nhiên và các sản phẩm có ứng dụng trị liệu và công nghệ sinh học hữu ích.
[ Làm rõ cần ] [ cần dẫn nguồn ]
Glycopeptide Linkage loại [ sửa ]
Polisacarit N-Linked [ sửa ]
Polisacarit N-linked lấy tên của họ từ thực tế là các polisacarit được gắn vào một
asparagin (Asn, N) dư lượng, và nằm trong số những mối liên hệ phổ biến nhất được tìm thấy trong tự nhiên. Mặc dù đa số các polisacarit N-liên kết mang hình thức GlcNAc-β-Asn
[6] liên kết cấu trúc ít phổ biến khác như GlcNac-α-Asn
[7] và GLC-Asn
[8] đã được quan sát. Ngoài chức năng của chúng trong gấp protein và tập tin đính kèm di động, các polisacarit N-thích của một protein có thể điều chỉnh chức năng của protein, trong một số trường hợp đóng vai trò như một công tắc on-off.
[5]
O-Linked polisacarit [ sửa ]
Polisacarit O-Linked được hình thành bởi một mối liên hệ giữa một loại axit amin chuỗi bên hydroxyl (thường là từ serine hoặc threonine) với polisacarit. Đa số các polisacarit O liên kết mang hình thức GlcNac-β-Ser / Thr hoặc GalNac-α-Ser / Thr.
[6]
Polisacarit C-Linked [ sửa ]
Trong ba mối liên kết ít nhất chung và hiểu ít nhất là polisacarit C-liên kết. C-liên kết liên quan đến các tập tin đính kèm kết cộng hóa trị của mannose đến một dư lượng tryptophan. Một ví dụ về một polisacarit C liên kết là α-mannosyl tryptophan.
[9]
Glycopeptide Tổng hợp [ sửa ]
Một số phương pháp đã được báo cáo trong y văn cho quá trình tổng hợp của glycopeptide. Trong những phương pháp chiến lược phổ biến nhất được liệt kê dưới đây.
Rắn giai đoạn peptide tổng hợp (SPPS) [ sửa ]
Trong SPPS có tồn tại hai chiến lược cho quá trình tổng hợp của glycopeptide, tuyến tính và lắp ráp tụ. Lắp ráp tuyến tính dựa trên tổng hợp các khối xây dựng và sau đó sử dụng các
SPPS để đính kèm các khối xây dựng với nhau. Bản đề cương của phương pháp này được minh họa dưới đây.
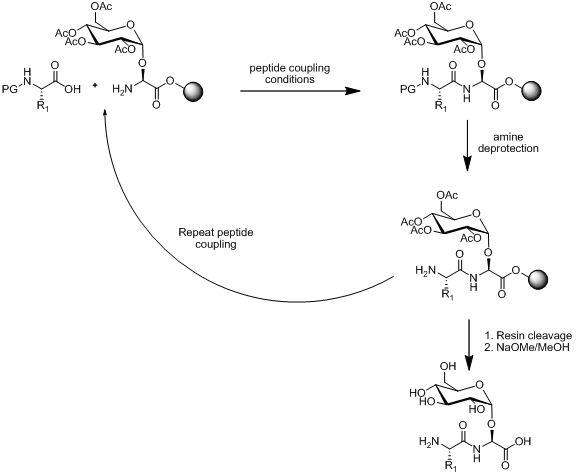
Đề án 1. Tổng quan về Chiến lược hội tuyến tính
Một số phương pháp tồn tại cho quá trình tổng hợp của khối xây dựng axit amin monosaccharide như minh họa dưới đây.
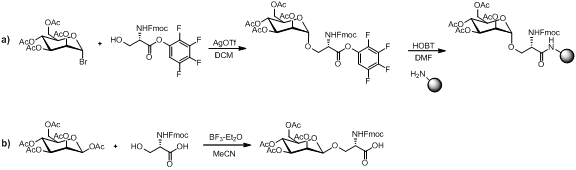
Đề án 2. a) Chuẩn bị các axit amin khối xây dựng monosaccharide trên nhựa
[10] b) Chuẩn bị của axit amin tự do khối xây dựng monosaccharide
[11]
Cung cấp các khối xây dựng axit amin monosaccharide là ổn định với điều kiện peptide khớp nối, điều kiện khử bảo vệ amin và nhựa tách. Lắp ráp tuyến tính vẫn còn là một chiến lược phổ biến cho quá trình tổng hợp của glycopeptide với nhiều ví dụ trong văn học.
[12] [13] [14]
Trong
lắp ráp tụ chiến lược một chuỗi peptide và dư lượng polisacarit là tổng hợp đầu tiên cách riêng biệt. Sau đó, polisacarit được glycosyl hóa lên một dư lượng cụ thể của chuỗi peptide. Cách tiếp cận này không phải là phổ biến như chiến lược tuyến tính do hiệu suất phản ứng kém trong bước glycosyl hóa.
[15]
Native Hóa thắt (NCL) [ sửa ]
Thắt hóa bản địa , hoặc NCL, là một chiến lược tổng hợp hội tụ dựa trên các khớp nối tuyến tính của mảnh glycopeptide. Kỹ thuật này làm cho việc sử dụng phản ứng chemoselective giữa một dư lượng cysteine N-terminal trên một đoạn peptide với một thio-ester trên C-ga cuối của đoạn peptide khác
[16] như minh họa dưới đây.
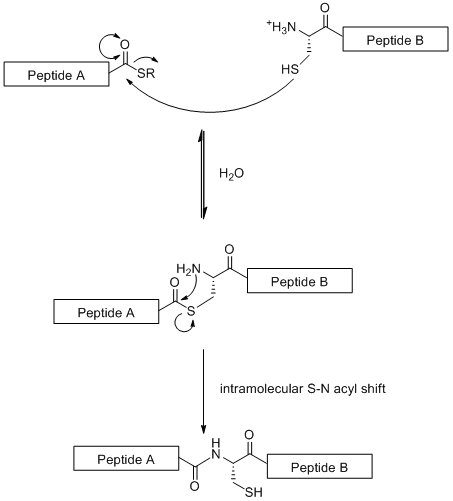
Đề án 3 Cơ chế của bản địa hóa thắt.
Không giống như các tiêu chuẩn SPPS (đó là giới hạn dư lượng axit amin 50) NCL cho phép xây dựng các glycopeptide lớn. Tuy nhiên chiến lược bị hạn chế bởi thực tế là nó đòi hỏi một dư lượng cysteine tại N-terminus, một axit amin dư lượng đó là hiếm trong tự nhiên.
[16] Tuy nhiên vấn đề này đã phần nào được địa chỉ của khử lưu huỳnh có chọn lọc các cặn cysteine một alanin.
[17]